北京博奥森生物技术有限公司品牌商
10 年
手机商铺
- NaN
- 0.10000000000000009
- 0.10000000000000009
- 2.1
- 2.1
推荐产品
公司新闻/正文
【文献解读】纳米颗粒增效放疗与PD-L1阻断协同作用以限制癌症术后的复发和转移
1238 人阅读发布时间:2022-06-30 13:47



为阐明手术和局部肿瘤生长之间因果关系的潜在分子机制,研究团队使用转录组学分析共鉴定出3823个差异表达基因谱。GO分析显示,差异表达基因在免疫相关功能和通路的生物过程中显著富集,提示手术创伤对免疫细胞具有很强的影响。值得注意的是,缺氧应激、促炎细胞因子、趋化因子和与免疫抑制相关基因在术后残留肿瘤显著上调,导致术后冷肿瘤形成,促进术后局部TME中肿瘤的复发和转移。
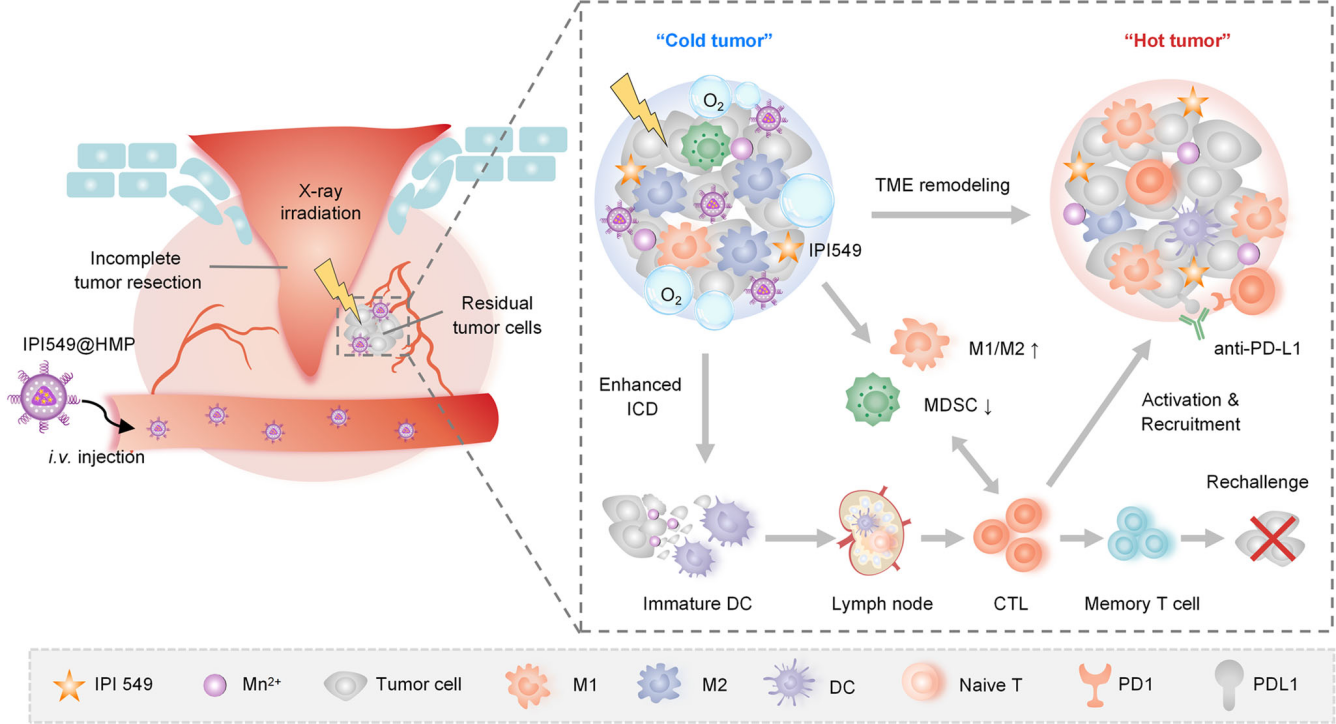
图1. 放疗免疫联合策略用于抑制术后癌症复发与转移的示意图
为了改善术后TME重塑对肿瘤治疗的不利影响,研究团队设计出一种IPI549@HMP纳米颗粒。一方面,其中的空心二氧化锰可以原位催化H2O2分解释放O2使局部缺氧得到缓解,同时其中搭载的IPI549可以有效抑制PI3-kinase γ信号通路,抑制髓源性抑制细胞 (MDSC) 向肿瘤中的迁移,阻断抑制性TME的形成,从而增强ICD以达到放疗增敏的作用,并能与PD-L1抗体阻断等产生协同抗癌作用。
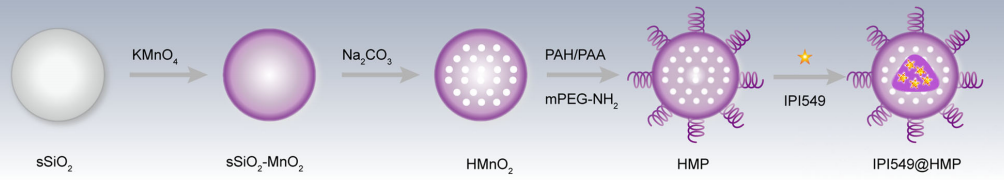
图2. HMP纳米颗粒合成和药物负载步骤的示意图
为了确认IPI549@HMP用于癌症术后辅助治疗的可行性,作者团队使用荷瘤小鼠模型开展了一系列研究。作为术后抑制性TME重塑的关键,局部缺氧的改善被视为首要的干预目的。首先,作者在体外证明IPI549@HMP可以在H2O2存在条件下,剂量依赖地增加环境氧气含量,并形成超声下可见的气泡(图3. b,c)。同时,乏氧缓解联合放疗处理后的细胞核中的DNA双链损伤标志物荧光信号显著上调,死亡CT26细胞数量大幅增加(图3. d,e)。随后,作者将IPI549@HMP静脉注射到荷瘤小鼠体内,光声成像结果显示IPI549@HMP在肿瘤组织内部大量富集,并提高了肿瘤组织中的氧饱和度。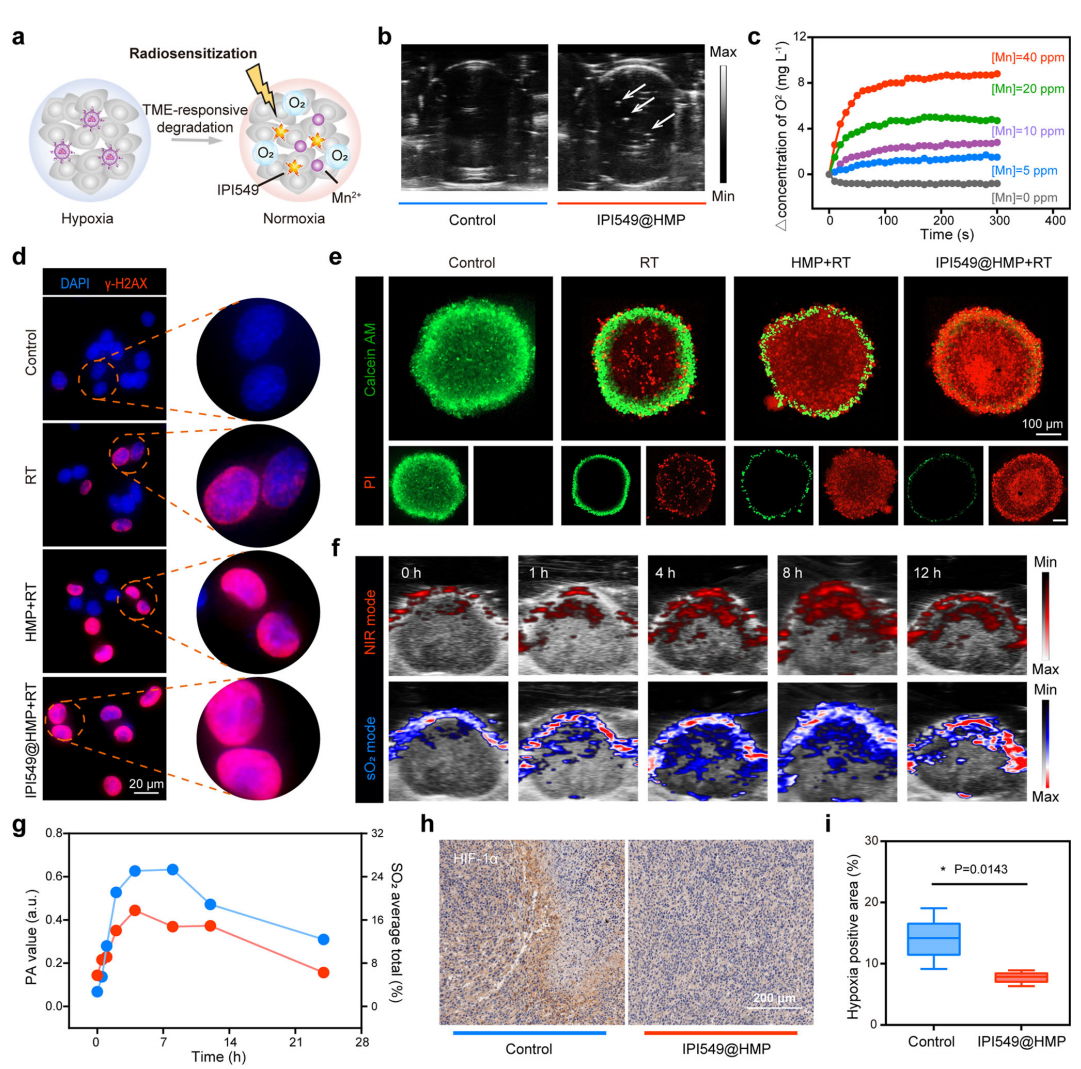
图3. IPI549@HMP诱导的乏氧缓解增强放疗疗效
为了进一步确认IPI549@HMP辅助治疗对肿瘤组织缺氧程度的影响,作者使用Bioss抗体,通过免疫组化检测了组织低氧诱导因子 (HIF-1α) 在肿瘤组织的表达情况。结果显示,IPI549@HMP辅助治疗后HIF-1α染色信号显著下调,阳性反应组织面积较对照组显著下降,说明基于IPI549@HMP的治疗确实缓解了肿瘤的缺氧状态(图3. h,i)。综上所述,IPI549@HMP具有良好的肿瘤富集和缺氧缓解能力。
相关产品信息
随后,作者通过大量的动物实验,证明IPI549@HMP能够增强术后放疗对荷瘤小鼠的治疗效果,增强ICD并延缓肿瘤进展。IPI549@HMP增敏的术后放疗能与PD-L1抗体起到疗效协同增强效应,加强ICB疗效。此外,IPI549@HMP还能诱发强烈的免疫记忆效应,使治疗后的小鼠能够耐受肿瘤再接种,从而防止术后癌症复发。 为了解决癌症对人类健康日益加剧的伤害和威胁,人们已经投入了相当多的努力和汗水用于寻找新的癌症治疗手段。癌症靶向药与免疫疗法的巨大突破使人们看到了攻克癌症的希望。然而,药物的耐药、响应率不高等问题仍然是摆在临床治疗面前的巨大障碍。近年来,纳米颗粒搭载实现的药物或核酸靶向递送技术正在兴起,本文团队在这一基础上,使用空心MnO2作为药物递送载体,从而使载体自身具有了通过改善缺氧而重塑免疫抑制性TME的能力。随后,配合小分子抑制剂、放疗、免疫检查点抑制剂等多管齐下,在小鼠模型中以极低的系统毒性,实现了癌症有效且长期的治疗。努力的汗水不应被一遍遍的重复实验所埋没,创意和灵感更需要信得过的试剂给予支撑。给博奥森一份信任,我们还你的不只是一支好抗体!参考文献
1.Chen, Q. et al. In situ sprayed bioresponsive immunotherapeutic gel for postsurgical cancer treatment. Nat. Nanotechnol. 14, 89–97 (2019).
2.Turajlic, S. & Swanton, C. Metastasis as an evolutionary process. Science 352,169–175 (2016).
3.Park, C. G. et al. Extended release of perioperative immunotherapy prevents tumor recurrence and eliminates metastases. Sci. Transl. Med. 10, 433 (2018).
4.Boussiotis, V. A. Molecular and Biochemical Aspects of the PD-1 Checkpoint Pathway. N. Engl. J. Med. 375, 1767–1778 (2016).
5.Bear, A. S., Vonderheide, R. H. & O’Hara, M. H. Challenges and Opportunities for Pancreatic Cancer Immunotherapy. Cancer Cell 38, 788–802 (2020).
6.Twyman-Saint Victor, C. et al. Radiation and dual checkpoint blockade activate non-redundant immune mechanisms in cancer. Nature 520, 373–377 (2015).
7.Neeman, E., Zmora, O. & Ben-Eliyahu, S. A new approach to reducing postsurgical cancer recurrence: perioperative targeting of catecholamines and prostaglandins. Clin. Cancer Res. 18, 4895–4902 (2012).